使用微流控技術為早產兒提供呼吸支持
對于早產的新生兒,呼吸系統發病率是一個重要的問題。早產新生兒的肺部尚未完全成熟,因此通常需要某種支持。盡管目前的治療方法(例如機械通氣)可大大降低死亡率,但它們可能導致醫源性傷害。由Selvaganapthy博士領導的麥克馬斯特大學研究小組與紐倫堡大學醫院合作開發了一種無泵微流控設備,以克服這些并發癥并為早產嬰兒提供呼吸支持。
作者解釋說:“在本文中,展示了微流控人工胎盤型新生兒肺輔助裝置(LAD)在新生仔豬模型上的首次成功操作,該模型最能代表早產嬰兒。”
微流控裝置的設計與工作原理
肺輔助設備(LAD)由8對連接到流量分配器的微流芯片(稱為微流血氧合器(MBO))組成。首先,血液進入流量分配器,流量分配器將流量分成相等流量的16個流。每個流都流入MBO,在此MBO進入的脫氧血液被氧化并離開設備。然后將這16個流合并并流到氣泡收集器中,最后返回動脈。
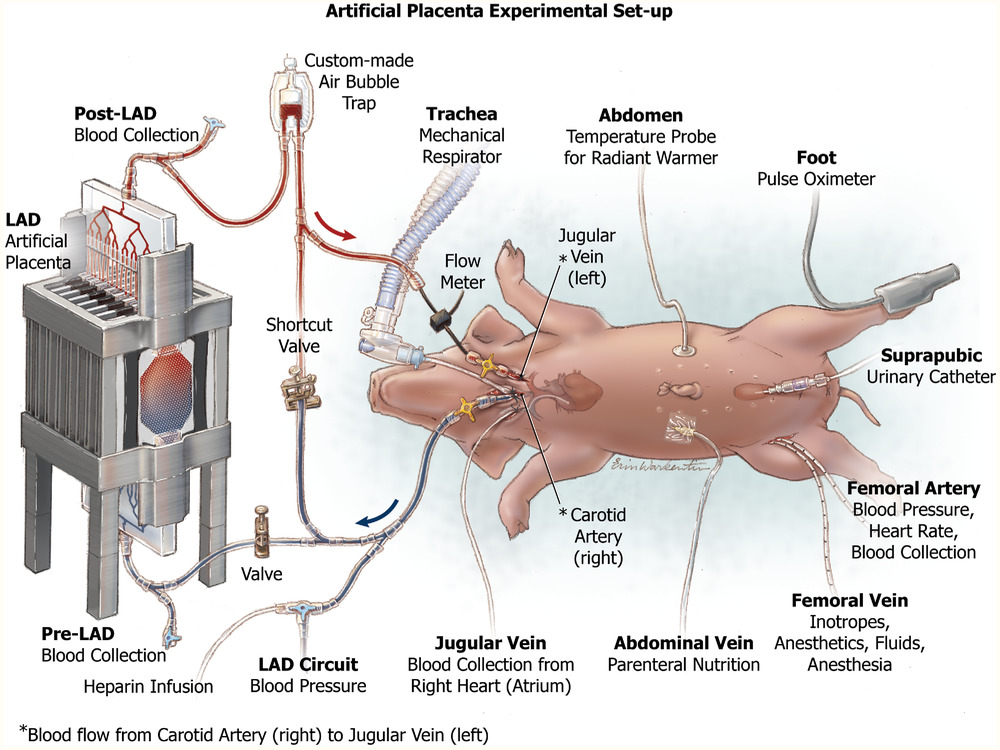
圖 新生兒仔豬模型的實驗裝置,用于測試用于人工胎盤的無泵新生兒肺輔助裝置。
“在我們的方法中使用的動靜脈連接將部分含氧的血液從肺部引導到LAD中。LAD可以通過將氧飽和度進一步增加到100%,然后再將其返回人體來提供幫助。計算表明,LAD能夠通過將其50 mL min-1的血液中氧飽和度從≈75%增加到室內空氣中的100%來支持1.5千克的新生兒,從而提供總氧需求的30%并防止呼吸苦惱。”
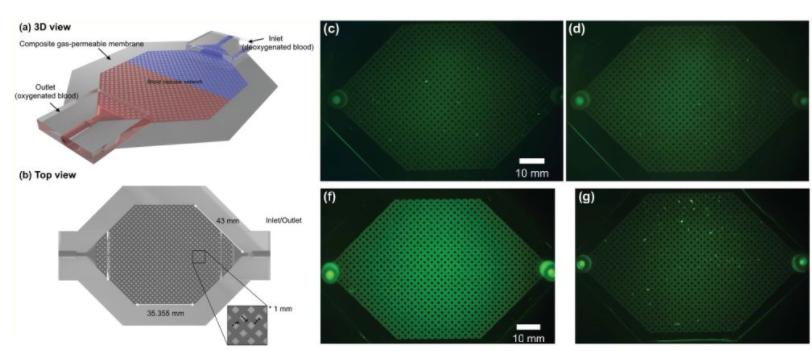
微流體血液充氧器(MBO)包括高度為180μm(或130μm )的PDMS微流體腔室,該腔室由1 mm 2的微柱陣列組成,總表面積約為30 cm 2。設計微流腔室,使輸入的血流分布在整個寬表面積上,以促進更有效,更快速地交換氧氣。微室夾在兩個多孔膜之間,以使氣體與周圍環境交換。
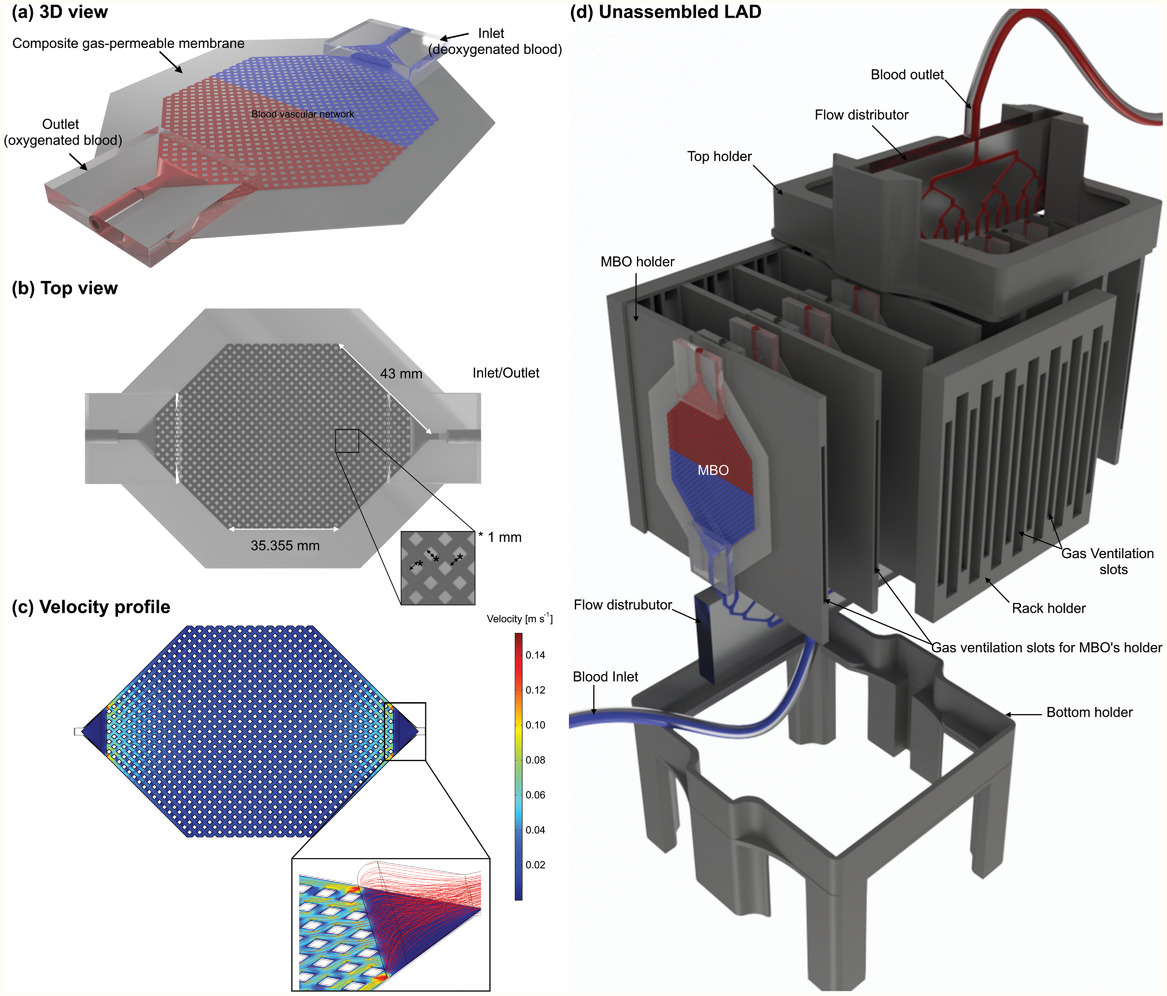
圖3、a)具有錐形入口/出口配置的MBO的3D示意圖,b)MBO的俯視圖,c)血液流速為5 mL min -1時MBO的速度分布圖,顯示了均勻的分布以及流動方向的緩慢變化d)LAD的3D圖以未組裝的格式顯示所有3D打印的組件,MBO和流量分配器。所有MBO之間都有固定的間隙,以使空氣對流流動。血液從底部流量分配器供入LAD,從頂部流量分配器離開LAD,以確保內部沒有氣泡。
微流體血液充氧器(MBO)包括高度為180μm(或130μm )的PDMS微流體腔室,該腔室由1 mm 2的微柱陣列組成,總表面積約為30 cm 2。設計微流腔室,使輸入的血流分布在整個寬表面積上,以促進更有效,更快速地交換氧氣。微室夾在兩個多孔膜之間,以使氣體與周圍環境交換。
已知PDMS具有疏水性,因此容易吸收蛋白質。因此,PDMS表面經常被修飾以防止蛋白質附著在表面上。在這種情況下,微通道用肝素包被以避免蛋白質吸收,血液凝結,血小板粘附和血栓形成。
在成功使用牛血對微流控肺輔助設備進行初步測試后,將其帶入了一個新的高度。擬議的微流體平臺已用仔豬進行了測試。選擇小豬作為動物模型是因為與其他動物相比,它在體重,血容量和生理特征方面更好地代表了人類早產和足月新生兒。
仔豬實驗的結果表明,這種LAD在無并發癥的氣體交換中是有效的,并且與體外結果一致。作者總結說,開發LAD的其他步驟包括安裝血液相容性,生物相容性以及通過臍帶血管進行發育。”
原文名稱:
A Pumpless Microfluidic Neonatal Lung Assist Device for Support of Preterm Neonates in Respiratory Distress
文獻鏈接:https://doi.org/10.1002/advs.202001860
- 上一條微反應器的特點與應用
- 下一條微流控技術中液滴主動聚并