骨髓芯片 Bone marrow–on–a–chip-骨髓造血干細胞的體外生物生理學
目前有關于造血干細胞的體外模型無法重現活體骨髓的細胞多樣性和復雜特征及功能,而與血液系統相關的大多數基因轉錄研究都是在活的動物體內進行的。本文描述了一種“骨髓芯片”方法可以實現在體外造血細胞微環境條件下培養活體骨髓。首先在體內工程化生成新的骨骼,再將其移植到體外充滿培養基的微流控芯片中。工程骨髓(engineered bone marrow, eBM)能在一周內保持造血干性和祖細胞之間比例正常。 eBM模型可進行器官級的骨髓毒性反應和藥物的保護作用的研究,而常規骨髓培養方法則不具備這樣的功能。這種仿生微型裝置提供了一種在體外分析骨髓中藥物反應和毒性,并可以用于體外造血和血液疾病研究的新方法。
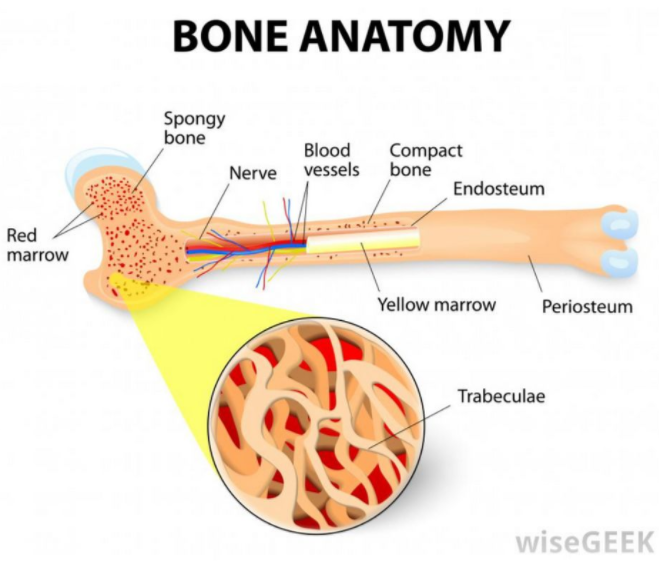
骨髓細胞微環境包括一系列復雜的維持造血系統可變性和功能的必須構成部分:化學分子、結構和物理刺激因子等。此造血細胞微環境調節著造血干細胞(hematopoietic stem cells, HSCs)在自我更新和分化,可制造成熟造血細胞以在體外重建擁有天然骨髓結構和功能的人造骨髓,如果能對其進行培養,則可以成為研究造血和測試新療法的有力平臺。
然而,已經證明難以在體外重現完整功能的造血細胞形成和維持所需的復雜骨髓微環境。雖然已經開發了各種體外系統來維持和擴大培養人源干細胞和祖細胞,但是目前還沒有在體外重建或研究完整骨髓微環境的方法。因此,造血研究通常依靠動物模型來確保完整骨髓微環境的存在,從保證正常的生理骨髓反應。此外,雖然已經報道骨髓能夠在體內工程化,但是在體外工程骨髓培養方法并沒有。為了彌合體內和體外系統之間的功能差異,研究者開發了一種生產包含人造骨和活骨髓的骨髓培養系統方法。首先在小鼠中產生骨髓,然后將其全部移植并在體外保持在微流體裝置內,接下來的方法如圖所示。為了探索可以整體移植人造骨髓的可能性,將具有中心圓柱形空腔(直徑1毫米,高4毫米)的聚二甲基硅氧烷(PDMS)裝置微型化,兩端具有開口,如圖1a中所示。我們的目標是設計可將填充植入物中的圓柱形內的類骨骼裝置,使其可以容易被全部去除,并插入到含有體外培養的類似體內形狀的室的微流控系統中(圖1a,b)。 這些初步研究導致在皮下植入4-8周后,在PDMS裝置內形成包含骨髓隔層的新骨。組織學分析顯示,骨髓主要由脂肪構成,并且即使在植入后8周(圖1c),其表現出低水平的造血細胞貢獻。組織學分析證實骨髓周圍厚度相對均勻的皮質骨存在,造血細胞占主導地位,脂肪細胞少(圖1c)。 eBM的組織學切片與完整股骨切片的比較結果說明,eBM的形態幾乎與天然骨髓的形態相同(圖1c)。
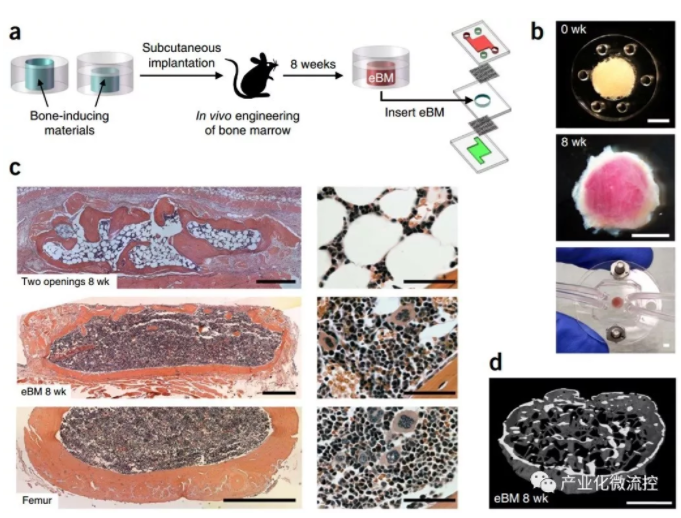
隨后還對工程骨髓的進行了體外培養、表征分析、并建立了體外輻射模型來進一步研究次骨髓芯片的功能。通過此種方法能夠產生同天然骨骼類似構造和組成的小梁骨,體重了一種制作預定尺寸和形狀的骨骼的方法,并且可以作為體外研究骨生物學的樣本,重塑了病理生理學的研究方法。
通過此種方法能夠產生同天然骨骼類似構造和組成的小梁骨,體重了一種制作預定尺寸和形狀的骨骼的方法,并且可以作為體外研究骨生物學的樣本,重塑了病理生理學的研究方法。因此,骨髓芯片是從血液學,腫瘤學和藥物發現到組織工程領域加速發現和開發廣泛生物醫學的有力方法。
(文章來源:文章作者陳有靈犀 轉自公眾號 產業化微流控 本篇文章內容源于emulate公司發表在Nature Methods Vol. 11 No. 6的文章 轉載僅供參考學習及傳遞有用信息,版權歸原作者所有,如侵犯權益,請聯系刪除)