一種新型微流體芯片裝置,能夠捕獲并分析腫瘤特異性細胞外囊泡
由麻省綜合醫院(MGH)的研究人員開發的一種新型微流體裝置可能實現腫瘤來源的細胞外囊泡(EVs)作為監測腫瘤對治療反應的生物標記物,這種通過血液傳遞分子的微小脂質顆粒能夠提供詳細的信息來指導治療選擇。在今年1月發表于Nature Communications雜志的文章中,來自MGH醫學工程中心(MGH-CEM)的團隊描述了從患有危險性腦腫瘤——多形性成膠質細胞瘤(GBM)的患者的血清或血漿樣品中捕獲EV的詳細過程、以及腫瘤特異性的遺傳和分子信息。
文章的通訊作者,MGH癌癥中心和MGH-CEM的BioMEMS資源中心的Shannon Stott博士說:“膠質母細胞瘤是一種極其致命的疾病,治療的選擇很少。由于腫瘤的位置特殊,獲得動態的實時分子信息一直有很大難度,這限制了我們確定腫瘤進展的能力,限制了患者去接受最新療法。我們的設備能夠從在血液傳送的數十億細胞外囊泡中挑選出腫瘤特異的細胞外囊泡,這可能會為這種和其他難以治療的癌癥類型帶來急需的新診斷和監測工具。”
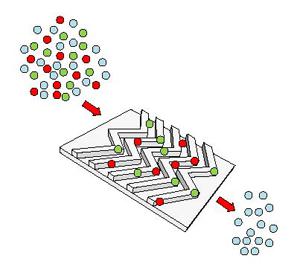
示意圖顯示了EV-HB-Chip的抗體包被的芯片表面如何從患者血清或血漿中捕獲紅色和綠色標記的腫瘤特異性細胞外囊泡。
在之前的研究中,分離細胞外囊泡的技術有限,將腫瘤的細胞外囊泡與其他非腫瘤細胞分泌的囊泡進行區分的難度很大。使用腫瘤特異性抗體的方法,耗時且麻煩,并且無法從樣品中捕獲足夠數量的腫瘤特異性細胞外囊泡。設計用于捕獲腫瘤細胞和分子的其他液體活檢技術 ,例如由MGH團隊成員開發的幾種循環腫瘤細胞(CTC)的分離裝置,在整個治療過程中監測腦腫瘤的能力也有限。由于這些潛在的生物標志物可能不一致能穿過血腦屏障,因此在血檢時它們的作用是有限的。
Stott博士的團隊將她開發的用于CTC檢測的HB芯片的功能與特定細胞外囊泡捕捉的功能相結合。將芯片的表面利用細胞外囊泡的物理特性進行了優化,芯片比電池小了幾千倍,并且含有在GBM細胞高度表達的蛋白質的抗體“雞尾酒”。該團隊還確定了一些其他因素,這些因素增加了從樣本中捕獲的腫瘤特定細胞外囊泡的數量,并開發了從該設備中釋放細胞外囊泡的方法,同時保留其內容以供詳細分析。采用這種方法,他們的裝置可以在1微升血漿液滴中分離出少至100個納米級大小的囊泡。
使用這種被稱為EV-HB芯片的新設備,研究人員分析了來自13名GBM患者和6名來自健康志愿者對照的血清或血漿樣品。EV-HB-Chip從所有13位患者中分離出腫瘤特異性EV,并在6位測試該突變的患者中的5位中鑒定出了EGFRvIII突變。被捕獲的EV中還鑒定出GBM的四種特征亞型中存在的基因,并揭示了超過50種癌癥相關基因的上調,有些基因在GBM EVs中以前未報道過。
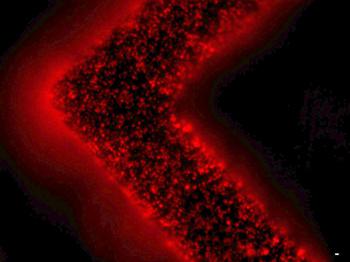
細胞外囊泡(紅色)從患者腫瘤細胞中釋放并被捕獲在EV-HB芯片表面。
作為哈佛醫學院助理教授,Stott指出,EV-HB-Chip具有極高的特異性和敏感性,可以使用相對較小的血液樣本中捕獲EV,這在其他血液活檢方法是不可能的,對兒科患者尤其有益。該裝置的靈活性應該使其可用于許多類型的癌癥,并且由于所有細胞釋放EV進入循環,其他疾病包括傳染病、自身免疫疾病、心臟病和神經退行性疾病等都可以應用。我們同時研究由EVs、CTCs和循環DNA提供的生物標志物,有助于確定哪些信息對于特定患者和治療階段最具信息性。
Stott指出,EV-HB芯片的設計是一種低成本、易于使用的設備,希望能夠迅速轉入臨床使用。“我們對這個早期階段的數據感到興奮,我們期待著擴大技術規模并增加分析的患者樣本數量。具體而言,我們有興趣探索這些囊泡如何隨著治療時間而改變,并且我們將我們的血液檢測看作是探索腦腫瘤患者的理想方式。”Stott說。
參考文獻:Reátegui E et al. (2018) Engineered nanointerfaces for microfluidic isolation and molecular profiling of tumor-specific extracellular vesicles. Nat Commun 9(1):175.
(文章來源: 外泌體資訊網 轉載僅供參考學習及傳遞有用信息,版權歸原作者所有,如侵犯權益,請聯系刪除)